De Nobelprijs voor de scheikunde gaat dit jaar naar de Amerikanen Frances Arnold en George Smith en de Brit Sir Gregory Winter. Ze ontvangen de prijs voor hun toepassing van evolutionaire principes op de ontwikkeling van eiwitten. Hun ontdekkingen zijn essentieel voor de productie van allerlei chemische stoffen, variërend van biobrandstoffen tot geneesmiddelen.
Evolutie zorgde ervoor dat diersoorten zich in de loop van de geschiedenis aanpasten aan hun veranderende omgeving. Gunstige genetische mutaties werden doorgegeven, terwijl ongunstige mutaties uitstierven. Dit is geen snel proces, een mutatie heeft ongeveer een miljoen jaar nodig om zich te settelen in een soort. De Nobelprijswinnaars van dit jaar hadden geen zin om zo lang te wachten en besloten de natuur een handje te helpen. Ze pasten de evolutionaire basisprincipes toe op de productie van eiwitten. Deze manier van werken wordt ook wel ‘gerichte evolutie’ genoemd.
Gerichte evolutie

Frances Arnold paste de methode voor het eerst toe op enzymen, eiwitten die chemische processen in lichaamscellen ondersteunen. Arnold wilde enzymen ontwerpen die hielpen bij het produceren van medicijnen, plastics en andere chemische stoffen. In de jaren tachtig probeerden wetenschappers enzymen kunstmatig te verbeteren. Enzymen zijn hier echter veel te complex voor, dus Arnold besefte dat er een andere invalshoek nodig was. Ze bedacht dat mensen dan wel niet in staat zijn om enzymen te verbeteren, maar de natuur zelf dit misschien wel is.
Relatie ontdekt tussen angst en rugklachten
Vrees voor pijn speelt een rol bij aanhoudende rugklachten, zegt bewegingswetenschapper Meta Wildenbeest.
Elk enzym hoort bij een specifiek gen. Arnold introduceerde willekeurige mutaties in de genen die hoorden bij het enzym dat ze wilde veranderen. Vervolgens plaatste ze deze genen in bacteriën, die hiermee duizenden variaties aan enzymen gingen produceren. Deze enzymen werden vervolgens allemaal aan een test onderworpen. De enzymen die het best presteerden hadden gewonnen en werden geselecteerd. Zij waren door naar de volgende ronde en het hele circus begon weer opnieuw, net zo lang tot de ultieme enzymen eruit kwamen rollen: mutate, test, select, repeat. Al in de derde generatie enzymen vond Arnold een variant die 256 keer zo effectief was als het originele enzym.
Technologen gebruiken deze methode tegenwoordig bij het fabriceren van allerlei chemische stoffen, van biobrandstoffen tot geneesmiddelen.
Behulpzame bacteriofagen

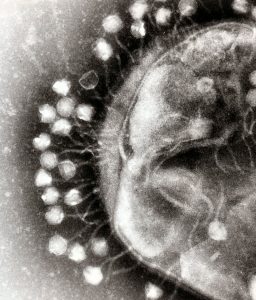
Het tweede deel van de Nobelprijs gaat naar wetenschappers die gerichte evolutie op een andere manier toepasten. Begin jaren tachtig wisten wetenschappers nog van weinig eiwitten bij welk gen ze hoorden. George Smith besloot bacteriofagen te gebruiken om deze puzzel op te lossen. Een bacteriofaag, of kortweg faag, is eigenlijk een heel simpel virusje. Het is een klein hoopje genetisch materiaal met een beschermend laagje eiwitten eromheen. Om zich voort te planten kaapt de faag een bacterie, die netjes kopieën maakt van het genetische materiaal en de eiwitten, en zo nieuwe fagen produceert.
Smith gebruikte eiwitten waarvan hij het bijbehorende gen wel al kende als een ‘capsule’. Hij verstopte stukjes onbekend DNA in de genen van een faag die hoorden bij deze capsule-eiwitten. De faag werd vervolgens gekopieerd, en op het oppervlak van de gekopieerde fagen verschenen nieuwe stukjes eiwit, als onderdeel van de capsule-eiwitten. Vervolgens bekeek Smith in welke capsule-eiwitten de nieuwe stukjes zich bevonden. Zo kon hij herleiden welke genen er bij welke eiwitten hoorden.
Vind je dit nog een beetje een vaag (faag) verhaal, beeld je dan in dat je per ongeluk een kookboek in de versnipperaar hebt gegooid. Enkele recepten heb je weten te redden, maar de rest van het boek is veranderd in losse aanwijzingen zoals ‘meng de ingrediënten door elkaar met een staafmixer’ en ‘zet de kom in een voorverwarmde oven van 180 °C’. Als je wilt weten wat het effect van deze losse aanwijzingen is op het uiteindelijke gerecht, kun je één van deze losse regels toevoegen in een bestaand recept, en kijken wat het effect is op je uiteindelijke gerecht. Het risico is dat je eindigt met een gepureerde pizza, maar in het gunstigste geval begrijp je een klein beetje beter hoe George Smith bekende recepten, genen, gebruikte om de functie van onbekende stukjes informatie te begrijpen.
Hengelen naar antilichamen

Sir Gregory Winter startte in de jaren negentig met het maken van medicijnen gebaseerd op antilichamen van mensen. Antilichamen zijn eiwitten die specifieke moleculen, virussen en bacteriën, die een gevaar voor het lichaam vormen, kunnen herkennen. Ze laten vervolgens de alarmbellen rinkelen zodat ons afweersysteem in actie komt tegen deze ziekteverwekkers.
Elk antilichaam bezit een Y-vormig hengeltje, dat bindt aan de ziekteverwekkers. Winter gebruikte Smiths fagen-methode om deze hengeltjes op het oppervlak van fagen tevoorschijn te toveren. Vervolgens ging hij aan de slag met de principes van gerichte evolutie. Hij bracht kleine veranderingen aan in de genen die hoorden bij de antilichamen, toverde zo nieuwe Y-vormige hengeltjes op het oppervlak van fagen, en selecteerde de antilichamen die het best een bepaalde ziekteverwekker herkenden.
Zo ontwikkelde hij in 1994 antilichamen die heel goed specifieke kankercellen konden herkennen. Dit leidde tot een doorbraak in de behandeling van uitgezaaide kanker. Maar de methode is ook succesvol bij auto-immuunziekten en gifstoffen.
Mis niet langer het laatste wetenschapsnieuws en meld je nu gratis aan voor de nieuwsbrief van New Scientist.
- DNA-mysterie opgelost: eiwitten vouwen strengen DNA op met heel veel lussen
- Bewegelijke wenkbrauwen belangrijk voor menselijke evolutie
- Nobelprijs voor de natuurkunde gaat naar pincetten en drilboren van licht
- Nobelprijs geneeskunde naar onderzoekers die veelbelovende kankertherapie van de rem haalden

