Als een muis een infectie heeft gehad, kan hij de opgewekte afweerreactie ‘doorgeven’ aan het nageslacht. Zo komen zij goed voorbereid ter wereld. Dit komt mogelijk door slimme aanpassingen aan het DNA in de cellen van het immuunsysteem.
De afweerreactie die muizen hebben opgebouwd tegen een schimmelinfectie kan worden overgedragen aan volgende generaties. Ook werkt het immuunsysteem van de nakomelingen over het algemeen beter, toont nieuw onderzoek aan. Zo blijkt opnieuw dat niet alleen DNA, maar ook ervaringen en omgevingsfactoren kunnen worden doorgeven aan volgende generaties.
Parate genen
Dit fenomeen komt waarschijnlijk tot stand door een proces dat epigenetica heet. Dat verwijst naar bepaalde markeringen op onze genen, die omkeerbaar zijn en het DNA zelf niet veranderen. ‘De meeste epigenetische processen beïnvloeden de toegankelijkheid van het DNA en bepalen zo in welke mate een gen actief is’, legt Marco Boks uit, psychiater en onderzoeker aan het UMC Utrecht en niet verbonden aan deze studie. Met andere woorden: hoe meer epigenetische markeringen op het DNA, hoe moeilijker het is om deze genen af te lezen en om te zetten naar werkzame eiwitten.
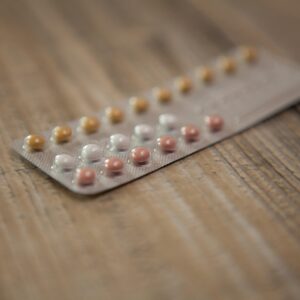
'De effecten van de anticonceptiepil verschillen per pil, per persoon en per dag'
Neurowetenschapper Anne Marieke Doornweerd onderzocht de effecten van de anticonceptiepil op het lijf en de gezondheid.
Bij planten en ongewervelden is al eerder aangetoond dat afweerreacties overdraagbaar zijn via zulke epigenetische markeringen. Nu is het voor het eerst ook in zoogdieren aangetoond.
Schimmelinfectie
Het internationale onderzoeksteam infecteerde mannelijke muizen eerst met de schimmel Candida albicans. Toen de dieren hersteld waren, paarden ze met gezonde vrouwtjes. De mannelijke nakomelingen werden vervolgens geïnfecteerd met E. coli-bacteriën. Hun immuunreactie werd vergeleken met die van nakomelingen van muizen die niet met de schimmel waren besmet.
‘De nakomelingen van de geïnfecteerde muizen waren significant beter beschermd tegen de bacteriële infectie dan het nageslacht van de niet-geïnfecteerde muizen’, zegt geneeskundige Mihai Netea van het Radboud Centrum voor Infectieziekten in het persbericht. Dit was ook nog het geval in de volgende generatie, de kleinkinderen.
Herprogrammering
De onderzoekers ontdekten dat een molecuul dat belangrijke delen van het immuunsysteem aanzet, actiever was bij nakomelingen van geïnfecteerde vaders. Ook waren de genen betrokken bij ontsteking actiever in deze nakomelingen. Dit kwam door een betere toegankelijkheid van deze genen in cellen die zich later ontwikkelen tot bepaalde immuuncellen, monocyten genoemd. ‘Dit laat zien dat deze voorlopercellen epigenetisch geherprogrammeerd zijn als de vaders eerder hersteld zijn van de schimmelinfectie’, aldus Andreas Schlitzer, immunoloog aan de Universiteit van Bonn.
Intergenerationeel
Om te onderzoeken hoe deze epigenetische veranderingen op de volgende generatie worden overgedragen, bestudeerde het team de toegankelijkheid en dus de genactiviteit in de spermacellen van geïnfecteerde vaders. ‘Hier was een duidelijke verschuiving zichtbaar’, zegt geneticus Jörn Walter van de Universiteit van Saarland. Zo vertoonden nakomelingen van geïnfecteerde vaders minder geblokkeerde genen in stukken van het DNA die bijdragen aan een goed werkende ontstekingsreactie en aan de ontwikkeling van monocyten. Hoe deze informatie vervolgens terechtkomt in het beenmerg, de geboorteplaats van veel immuuncellen, is nog niet bekend.
Aanpassingsvermogen
Organismen passen zich aan als hun omgeving verandert. De klassieke evolutietheorie stelt dat dit komt door langzame veranderingen in het DNA zelf. De resultaten van dit onderzoek pleiten voor een andere verklaring: organismen passen zich continu aan hun omgeving aan met behulp van epigenetische markeringen, die op hun beurt de genactiviteit beïnvloeden. Dit is in ieder geval zo in muizen; de onderzoekers weten nog niet of hun bevindingen ook op mensen van toepassing zijn. Maar daar gaan ze wel van uit, zegt Schlitzer. ‘De mechanismen en immuuncellen van muis en mens lijken veel op elkaar.’
‘Netea en collega’s presenteren sterk bewijs dat er overdracht is van aanpassingen aan de omgeving – in dit geval het risico op infectie – van ouders op kinderen. Dat is evolutionair goed te begrijpen, want het is handig om goed voorbereid ter wereld te komen’, reageert Boks. ‘Het is een fijne gedachte dat zoogdieren zich op deze manier kunnen aanpassen aan veranderende omgevingen. Dat kan wellicht bijdragen aan het terugdringen van ziektes gerelateerd aan het postindustriële tijdperk, zoals obesitas en diabetes.’

